高效水处理的高级氧化工艺研究进展
Nirmalendu Sekhar Mishra1* ,rajesh reddy.1
,rajesh reddy.1 , Aneek Kuila1
, Aneek Kuila1 ,ankita rani.1
,ankita rani.1 , Priya穆克吉1
, Priya穆克吉1 ,艾哈迈德谢里夫1
,艾哈迈德谢里夫1 和萨拉万南·匹亚岛1
和萨拉万南·匹亚岛1
1印度理工学院环境科学与工程系,印度恰尔肯德邦丹巴德826004。
DOI:http://dx.doi.org/10.12944/cwe.12.3.02
复制以下内容以引用本文:
高志强,王志强,王志强,等。高级氧化技术在水处理中的应用研究进展。Curr World Environ 2017;12(3)。DOI:http://dx.doi.org/10.12944/cwe.12.3.02
复制以下内容以引用此URL:
高志强,王志强,王志强,等。高级氧化技术在水处理中的应用研究进展。Curr World Environ 2017;12(3)。可以从://www.a-i-l-s-a.com/?p=1054
文章出版历史
| 已收到: | 2017-11-24 |
|---|---|
| 公认: | 2017-12-16 |
介绍
由于不适当的水管理,地球的淡水资源急剧枯竭或受到污染,导致脆弱的局势。另一方面,由于人口的指数增长和传统处理方法的无能为力,对安全饮用水的需求日益增加。1根据当地标准,这些传统和现代净化技术可用或实践,用于在本地标准和这些跨度从基本过滤,吸附到最先进的技术;膜分离和先进的氧化过程(AOPS)。在现代之后,后者被认为是在不含有机物,无机和微生物的安全饮用水中提供高效的。2、3由于AOPs具有很强的活性氧生成能力,它被认为可以用于处理不同类型的水和废水,包括内分泌干扰物(EDCs)、持久性有机污染物(POPs)、总有机碳(TOC)和微污染物。4,5该AOP是一种广泛的分类,其中包括用于产生反应性氧物质的各种技术,如图1所示。通常,任何水净化技术的现实目的是使水无毒的物质(有机,无机和生物学)。在这方面,AOP的特征是涉及羟基自由基产生的最佳水处理/纯化过程(*(OH),足以在标准温度和压力下影响水的净化。6AOP对所有现有化学和生物过程的显着优势是它们完全“环保”,因为它们既不将污染物从一个相到另一个相位(如化学沉淀和吸附),也不会产生大量的危险污泥。7 - 10在20世纪80年代初提出了全规模的基于AOP的水净化/治疗,并报告了相当大的成就。11,12.因此,本综述将强调AOPS的各个方面,以实现有效的水管理。
 |
|
不同AUOP各类污染物的增强降解引起了各种研究社区的关注。AOP可以通过不同的方法原位产生各种活性氧(ROS),例如Sonoly解水,臭氧,UV,FENTON工艺等。这些ROS随后用于各类污染物的降解。已经赋予了对不同AOP的过程参数和劣化的见解。因此,本文巩固了各种研究人员报告了有效水资源管理的重要作品。
Sonolysis.
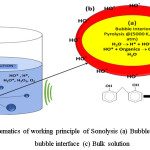
它涉及到频率范围为20 KHz -10 MHz的超声波的有效利用。13,14它不利用任何危险化学品作为Mediator的危险化学品,因此被视为Eco友好的过程。由于超声波/流体动力学的结果形成的空化气泡的爆炸,有机分子降解。产生的空化气泡倾向于在其尺寸中波动,直到在它们的共振尺寸下塌陷,导致储存储存的能量导致爆炸。13这些空化气泡的形成高度依赖于超声频率。15通常,由于在塌陷气泡中存在高水蒸气含量,较低频率导致形成活性气泡的较小浓度。15然而,高频率会导致活性气泡之间的碰撞,产生较少的反应物质,导致效率降低。15声解析的工作原理示意图如图2所示。
这些气泡的爆炸导致污染物通过极压和温度(分别为500-10,000atm和3,000 k)的热解16、17随后导致了*哦,通过解离水分子。由此形成*OH进一步与污染物发生反应,形成最简单的形式。18、19气泡液界面的降解由此主导*哦。而且,自由基从气泡 - 液界面迁移到散装液中导致其中的二次反应。它是不含额外产生的二级污染物的污泥的自由过程,将其促进作为光解,光环和芬顿工艺等最优选的技术之一。14此外,它具有处理混浊水的固有能力,导致挥发性和少量可溶性有机物的有效降解,导致高浊度。19然而,由于较高的能源消耗和较低的矿化效率的限制,其生存能力较低,这就导致了其他各种AOPs的强化,如光催化(声-光催化),光-fenton(声-fenton),臭氧分解(声-臭氧化),声光解等。
 |
|
矿化效率也可以通过改变操作参数如初始基质浓度、pH、催化剂负载和超声功率来提高。20.在强化的过程中,声光解涉及在无催化剂的情况下,紫外线照射和超声波对污染物矿化的协同作用。然而,声光催化涉及在半导体光催化剂的存在下使用紫外线照射和超声波。紫外/超声波的协同作用增强了活性自由基的生成,提高了矿化效率。这种增强的生成归因于半导体光催化剂中激发形成的电子-空穴对。21.另外,光催化剂的存在改善了气泡空化现象,导致反应物质朝向液体区域的增强迁移。21.因此,由于超声在过氧化物物种上,引起上述方法的强化导致自由基的浓度增加。22.在Sono-ozonolics的情况下,传质转移*OH和臭氧增强,导致H的原位生成2O2/ HO*(每个O3.分子降解产生2*哦)22.导致污染物的有效矿化。反应产物是由水中的空化现象和臭氧的热分解产生的。通过增加压力或加入过氧化氢,矿化可以进一步增强。23.该组合有助于在pH值为5.5 - 6.5的范围内实现效率水平> 80%。24.
臭氧化
臭氧被分类为强氧化剂和强大的消毒剂25.氟过后。据报道,理论上臭氧氧化无机和有机污染物,但实际臭氧对污染物具有高度选择性。25.因此,臭氧被认为是在其反应中具有高选择性的亲电试剂。26.臭氧水处理对微生物降解具有很高的适用性,26.脱色,27日、28日微核性塑料去除,29、30non-protonated胺26.和味道和气味去除。26,31该技术已在瑞士、德国等欧洲国家作为氧化剂和污水处理厂进行商业应用。32.臭氧发生器、臭氧发生器的冷却系统、对加入臭氧发生器的空气进行脱水的预处理装置和去除废气中多余臭氧的后处理反应器是实施臭氧化所需要的装置。33.典型臭氧反应器的原理图如图3所示。
![图3:臭氧化的典型反应器组件。(A =液体循环泵; B =臭氧液分析仪; C =臭氧气体分析仪)[34]。](http://www.a-i-l-s-a.com/wp-content/uploads/2017/12/Vol12_No3_rev_Nir_Fig3-150x150.jpg) |
|
臭氧水相反应
在水中,臭氧是不稳定的,因此与水的成分发生反应。25.臭氧在水中的分解机制与复杂的原子顺序和单电子输运有关*OH的生成,进一步涉及OH的生成-,何2阿,2-阿,3.-,何3.哦,哦2和何4实体如图4所示。臭氧分解过程可以通过提高pH值或过氧化氢浓度来加速。26.众所周知,臭氧是水中的主要消毒,而OH和O3.两者都作为氧化剂在氧化过程中的水与O3.高度选择性和*OH的反应性很强。26.因此,臭氧氧化可同时用于消毒和氧化。初始阶段水中臭氧浓度迅速下降,服从一级动力学;第二阶段臭氧通过氧化而下降,服从二级动力学。26日,35岁的36
![图4:水基质中的臭氧反应[25]](http://www.a-i-l-s-a.com/wp-content/uploads/2017/12/Vol12_No3_rev_Nir_Fig4-150x150.jpg) |
|
溶解的臭氧的半衰期根据水而异。26,28,37pH,碱度,天然有机物质含量。26,28其中天然有机物可与臭氧反应或清除*即直接或间接影响臭氧稳定性。26.据报道,臭氧有效地与直接或间接的物质反应*哦,即使中性pH作为过氧化氢,超氧化物离子。25.臭氧,*OH或两者的混合,并包含贯穿臭氧化的有机和无机化合物。像-CH这样的供电子基团能增强臭氧氧化3.阿,-哟,3.26,32被-Cl, -NO等吸电子基团还原2。26.硫化物基团和含有氨基和双键的化合物也表现出高臭氧的反应性,而在臭氧过程中与饱和化合物的反应性低。26.臭氧与甲基和乙醚的反应活性也很低。其次是二电子氧化,将氧原子从臭氧中释放出来,用于氧化无机化合物。26,38,39由于亲核性降低,氧化电位随物种的质子化而降低。26.因此臭氧化可以有效地应用于各种污染物,如表1所示。
表1:臭氧化降解的各类污染物
S.NO. |
类别 |
污染物 |
参考。 |
1) |
微生物(蓝藻)产品 |
微囊杆菌-LR. |
[40] |
2) |
农药 |
Carbofuran. |
[41] |
地乐酚 |
|||
3) |
溶剂 |
氯乙烯 |
42(26日) |
Dichloroethenes |
|||
4) |
配体 |
Nitrilotriacetate (NTA) |
[43] |
Ethylenediaminetetraacetate (EDTA) |
|||
5) |
制药 |
Dichlorofenac |
[44] |
卡巴马嗪. |
|||
BenzafBribate. |
|||
双氯芬酸 |
|||
布洛芬 |
|||
磺胺甲恶唑 |
|||
罗 |
|||
Iopromide |
|||
17α - 乙基雌二醇 |
|||
6) |
烯烃 |
[42] |
|
7) |
Deproteinated胺 |
[45] |
|
8) |
无机微污染物 |
Fe(ii) |
[46] |
CN- |
|||
锰(II) |
|||
H2年代 |
|||
没有2- |
工艺条件的影响
在较低的溴化物浓度下,较高的pH值下臭氧投加量可提高微污染物的减排效率。29.而低碱度和低溶解氧浓度降低了系统的氧化能力。26.适用于双氯芬酸、磺胺甲恶唑、卡马西平、甲氧苄氨嘧啶、氢氯噻嗪、苯那酮、曲马多、美托洛尔等含臭氧的活性化合物*OH不受pH变化的影响,降解效率不变;然而,升高的pH值容易转化O3.导致耐臭氧的削减。29.
臭氧化限制
臭氧对氯化苯、土臭素、甲基异龙脑、三卤甲烷等有低氧化作用。25.隐孢子虫paravum卵囊是一种抗消毒的微生物,需要更多的臭氧暴露,因此在饮用水中形成不良的副产物点,47岁由于臭氧具有较弱的氧化电位,故其对氨的去除速度较慢。26.人们已经看到,臭氧氧化产生的氧化产物可能含有未知的有毒物质,但与具有微不足道的抗菌和雌激素活性的亲本化合物相比,这些氧化产物的浓度很低。有毒物质包括甲醛、酮类、酚类、硝基甲烷和致癌物质,如溴酸盐、n -硝基二甲胺(NDMA)。32岁的48溴酸盐是一种潜在的致癌物,当臭氧和*OH在液相中与溴反应。除了臭氧的所有高成本外,作为试剂,是实施臭氧化的主要限制因素。
O3./小时2O2
臭氧与过氧化氢结合已成为水处理领域的一个新领域,它能比单独处理更有效地氧化无机和有机物质。首次研究利用O3./小时2O2由Nakayama等人和Hango等人同时进行。同时,深色的出版社。和Duguet出版社。,performed for treating drinking water.51.研究表明H2O2臭氧化的应用增强了有机物和三卤甲烷前驱体的氧化。它的加入增加了臭氧转移速率,51,52-56由单个电子转移形成HO2-这引发了臭氧分解周期形成*哦。H2O2臭氧氧化尤其提高了脱色效率,但处理饮用水、农药、芳香族化合物和氯化溶剂的氧化主要应用O3./小时2O2,61的好处啊3./小时2O2使用包括较短的反应时间,允许在反应器出口处高度施加臭氧剂量和臭氧的低聚。处理条件如反应时间增量在臭氧添加后,加强pH和施加过氧化氢施加过氧化氢可以增强臭氧的氧化性能。然而,反应时间和pH的增加却在经济上不可行2O2作为饮用水处理最常应用的低成本试剂,以实现更高的效率。h臭氧分解2O2成立法团由*哦和超氧化物形成。26.如果使用常规臭氧处理和o处理表面水域3./小时2O2臭氧向HO的转化没有明显的差异*.但在地下水的情况下,含有对氯苯甲酸(PCBA)通过常规臭氧的氧化是20%,通过掺入H增加到50%2O2随着阿3..26.藻类产生的土臭素和2-甲基异布尼醇(MIB)等化合物由于含有饱和环系,也很难被臭氧氧化。然而,它们很适合用O3./小时2O2具有高的氧化速率常数[26]。溴酸盐的形成是低氧的3./小时2O2比传统的臭氧化过程。51.
O3./催化剂
在臭氧处理过程中加入均相和异质催化剂也在提高氧化反应方面发挥关键作用。57.类铁金属氧化物2O3.,艾尔。2O3.加,TiO2-me,mno.2,茹/首席执行官2以及铁等金属离子2+、铁3+、锰2+等被用作催化剂。57.通过铁和锰的结合成功地去除了化学需氧量、有机氯化物和总有机碳。57,58像O.这样的组合3./ TiO2,茹/首席执行官2/ O3.,33.艾尔2O3./ O3.对总有机物[57]的去除效果较好。颗粒活性炭也被认为是破坏生物难降解化合物的催化剂.57,60
UV基地AOP.
紫外光处理一般作为三级处理来杀灭微生物和降解那些能吸收紫外光的水生有机物。在紫外光的吸收下,污染物中的电子从基态激发到激发态(方程)。1)从那里电子转移到一个氧分子,这个氧分子将两个O转化2和污染物分子形成一个自由基(方程式)。自由基是一种高度活性的物质,它氧化其他分子以获得稳定的形式。
P→P * ...............................(1)
p * + o2→P+ *+O2- *.....................( 2)
紫外线还可以导致污染物的化学键的均分割切割,从而产生两个基团(方程。3)。波长小于190nm的UV光可以有效地打破高度稳定的C-F键,而210-230nm的波长可以破坏C-Cl键。形成的基团然后可以与氧气(方程4)反应,或者可以参与与其他溶解分子的进一步氧化还原反应。
r→x→r*+ X*.................( 3)
R*+ O.2→反渗透2............................( 4)
波长小于190 nm的高能紫外光可以光解水分子形成*哦(方程。5),然后氧化其他有机底物。61.
H2O + hv→2HO*..........................(5)
像汞弧像不同的紫外线发光强度的灯用于产生UV辐射。这些通常具有三种类型:低压,中型和高压灯。前者是单色的本质上,发出波长253.7nm的光。中高压灯在紫外线区域发出各种波长,并且由于其更高的强度而渗透,并且需要更少的时间来完成处理。对它们的应用的限制是它们是能量密集型的。62.像脉冲辐射灯和准分子灯也被用来产生紫外线照射。63.紫外线处理系统的主要组成部分包括灯具、镇流器和电抗器。汞弧光灯一般作为UV灯使用。镇流器是一种支撑装置,主要有两种功能:一是为灯的可靠启动提供适当的电压;其次,他们保持一个连续的电流流向灯,以防止灯短路。最后,反应器,它们有两种类型:接触式和非接触式反应器。接触反应器是紫外灯保持在水下状态的反应器。为了防止损坏,灯通常被密封在石英套管中。非接触式反应器是一种在水样和灯之间放置透明材料的反应器。灯可以垂直或平行于废水流动的方向。62年,64年该工艺的主要优点是环保,处理时间短。它也不需要使用化学品;因此,在处理后没有残留产品。62.该技术已被应用于许多有机化合物的降解,包括内分泌干扰物和各种工业溶剂。这是一种高效降解NDMA (n -亚硝基二甲胺)的方法。65 - 67Sakai等人(2012)发现222 nm Kr-准分子- UV灯是替代低压(LP)和过滤中压灯(FMP)降解NDMA的更好选择。68.Sanches等人2010年利用低压紫外灯检查了五种农药的降解情况,即甲草胺、阿特拉津、迪隆、五氯苯酚、氯苯磷和异丙隆。除异丙隆外,常规低压汞灯可降解50%以上的农药。异丙隆虽然具有较高的摩尔吸收系数,但其量子产率较低,这可能是其降解较低的一个原因。69.表2总结了UV光解法处理的各类污染物。
表2:UV光解处理的各类污染物
类别 |
特定的污染物 |
参考。 |
追踪有机化学 |
NDMA (N-nitrosodimethylamine) |
[68] |
药品 |
双氯芬酸,反紫红素,氯化丁酸碱,诺福克西林,咖啡因,双吡啶胺,Diltiazem,Cloficric酸,acetamiprid |
[70] |
磺胺甲恶唑(SMX)、土霉素(OTC)和环丙沙星(CIP) |
[71] |
|
Ditrizoate |
[72] |
|
农药 |
阿特拉津,利裔,阿尔兰,五氯酚,氯苯酚 |
[69] |
合成雄激素类固醇 |
去氢睾酮 |
[73] |
EDC |
Butylparaben |
[74] |
该技术的局限性是*OH由UV的作用形成,有时会导致有机污染物的部分降解,在CO的地方留下更高水平的中间体浓度2和H2O.较高浓度的总悬浮固体(TSS)和颗粒材料(例如腐殖化合物和铁)滞后。此外,与氯化物这样的其他三级方法相比,它是能量密集且昂贵的。62.
UV / O.3.过程
UV和O结合处理3.是一种成熟的先进氧化技术。这种技术比单独的UV和O更有优势3.技术原因是它结合了两者的优势。紫外线与臭氧接触(O.3.)打破它形成*OH,通过以下反应步骤75.:
O3.+ H.2o + HV→H2O2+ O.2.......................( 6)
H2O2+ HV→2oh*.......................( 7)
2o3.+ H.2O2→2哦*...........................(8)
的*OH形成,然后完全矿化有机物形成CO2或H.2O或形成一些容易降解的中间物质。作为一种不稳定的反应性分子,O3.在实验中,气体是在原位生成的。因此,生成的O3.然后将安装UV灯的反应器喷射到其中。75,76.这些紫外线灯被密封在接触反应器的石英套管内,以确保更好的紫外线传输。在非接触式UV灯与废水由透明分离器分开。紫外线反应器的结构示意图如图5所示。
![图5:由两个UV库组成的UV反应器示意图[77]](http://www.a-i-l-s-a.com/wp-content/uploads/2017/12/Vol12_No3_rev_Nir_Fig5-150x150.jpg) |
|
在大多数研究中,都发现UV/O3.除了其污染物降解能力之外,治疗成功,COD降低。75,78-80.在Hassan等的一项研究中。al。(2017),发现UV / O的颜色去除较高3.与O3..80Tehrani et。al。(2010)通过UV / O研究了反应性蓝19染料的去除3.和O3.治疗。在他们的研究中,发现UV/O3.治疗在鳕鱼中比o更有效3..随着染料初始浓度的增加,脱色率降低。78.影响处理效果的因素有:pH值、污染物初始浓度、溶液浊度、O含量3.剂量、紫外线剂量、过程中使用的紫外线灯类型、反应时间、水中存在的清除剂。80-82表4通过uv / o有效地删除了一些选定的污染物3.治疗
表3:UV/O去除的选定污染物3.治疗
类别 |
具体污染物 |
参考 |
染料 |
RB-19 |
[79] |
DB-86. |
[80] |
|
MV-40 |
[81] |
|
直接黄色50. |
[82] |
|
苯酚 |
4-Chlorophenol |
[83] |
药品 |
酮洛芬 |
[84] |
咖啡因 |
[85] |
|
农药 |
林隆 |
[86] |
其他有机化学品 |
Nitrosopyrollidine |
[87] |
双酚A |
[88] |
Fenton流程
芬顿反应是最重要的AOP之一,与之相关的化学反应包括过氧化物反应(H2O2)有fe.2+生成可降解水相中有机及无机物质的活性氧。芬顿化学可以追溯到1894年,当时H2O2据报道,通过亨利J.Fenton氧化酒石酸氧化亚铁盐。89.1934年,它是由Haber和Weiss提出的90.有一种形成*因为芬顿反应。这*哦,氧化潜力为2.73V。因此,它是最活跃和最强大的氧化剂之一,可用于大多数有机化合物的降解,包括新兴.91
均匀的芬顿反应
FENTON方法是一种简单且经济的方法,用于产生高活性氧气用于降解污染物。H2O2安全且易于处理,比较便宜,易于分解到水和氧气中。同样,铁也更便宜,使用安全。这种分解的机制2O2后来由Barb等人进行了修订。92-94.介绍芬顿法的链式反应。所提出的机制涉及H2O2生产*OH /自由基是在黑暗条件下酸性介质中七个反应的序列。95.反应如下:
菲2++ H.2O2→铁3++哦−+*哦 ..........................( 9)
菲3++ H.2O2→铁2++何·2+ H.+...........................................(10)
*OH + H.2O2→何·2+ H.2O .............................( 11)
*哦+铁2+→铁3++哦−................................(12)
菲3++何·2→铁2++ O.2H+.................................(13)
菲2++何·2+ H.+→铁3++ H.2O2..............................(14)
何·2+何·2→H2O2+ O.2...................................(15)
*OH,是污染物降解所需的氧化剂,由反应产生9。因此,反应10变成了限速反应,因为它比反应慢了几个数量级。有机化合物(RH / R)可被下列任何一种或组合氧化:(1)*OH,(2)氢(R*),(3)添加羟基(*卢武铉)。96.
RH +*哦→H2o + r *→进一步氧化..................(16)
R +*哦→*Roh→进一步氧化..............................(17)
*OH,可以被任一铁清除2+或H.2O2如等式10和11所示。因此,优化Fe2+/ H2O2是为了减少腐食而携带的吗·哦。而产生的铁3+沉淀形成铁氧氢氧化物,当pH值从最优值增加时产生不良污泥,在实际应用中产生问题。97,98另外,用于大规模废水处理的芬顿工艺的应用包括pH依赖性(仅在pH 2至5的范围内有效),产生铁基污泥,其昂贵后处理的必要性,最终中和处置前处理的水。99.因此,光Fenton等改进的Fenton工艺需要进一步的研究,光Fenton可以通过光照射提高反应速率。有时使用螯合剂可为芬顿反应提供最佳pH值。螯合配体与氢氧根离子竞争有利;因此增加化合物可溶的pH值范围。在最佳ph值下,反应动力学类似于芬顿氧化3+-CIP螯合物,去铁氧胺,环糊精,氮三乙酸(NTA)和乙二胺四乙酸(EDTA)100-103被采用。然而,需要额外的研究来鉴定可以增加氧化,稳定性和生态友好速度的螯合剂。
Photo - Fenton法
紫外和可见光照射芬顿反应溶液,可提高反应速率和降解效率。99.效率的提高与Fe的光化学性质有关3+复合体[FE.3+(哦)-]+和[fe.3+(有数2)-]2+解离Fe2+.铁的光化学性质3+由于减少的Fe,对Fenton流程提供了优势2+与H反应2O2形成*根据反应9。104光- fenton反应在pH = 2.8时达到最佳反应条件,当pH高于此值时,铁离子含量增加3+当pH降低到最优值以下时,Fe(OH)的浓度2+将下降。105过氧化氢在紫外光照射下发生光解,如式18所示:
H2O2+Hν→2HO*................................( 18)
虽然反应10中双氧水光解的量子产率较好,但由于H对光的照射吸收较弱2O2,其在光芬顿反应中的活性不显著。与Fenton类似,photofenton的缺点是污泥处理成本高,pH范围要求窄,限制了其在废水处理中的应用。97106年
异构催化剂
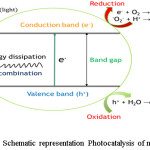
多相光催化不同于其他同时涉及氧化和还原的处理方法,使用光照射和光吸收光催化剂。各种化合物可以利用光照射催化光解产生氧化还原反应。这些化合物通常具有空导带和充满价带的能带结构。89.一旦光照射入射在半导体上并且如果光子的能量超过半导体的能隙,则电子从价带激发到留下孔后面的导带。90年,91年价带中的活性电子和传导中的空穴与水发生反应*哦,超氧化物(*O2-)及过氧化物自由基(*哦)。这些自由基进一步降解各种污染物,得到产物,如一氧化碳2和H2O。92-94图6中示出了光催化和污染物降解的机理。
 |
|
异源性光催化剂材料由TIO组成2,Zno,Fe2O3.,WO.3., SnO2,zro2,cds zns等其中,tio2是目前应用最广泛的异质光催化剂,具有易于获得、价格低廉、化学稳定性高等优点。另一类光催化剂也进行了适用性试验。由于可见光利用的局限性,在传统的光催化剂材料中掺杂了合适的助催化剂。表4显示了用于废弃物降解的各种杂化多相光催化剂。
表4:用于降解不同污染物的各种光催化剂
| Sl。不。 | 光催化剂 | 污染物 | 删除效率 | 参考。 |
| 1. | 氧化石墨烯/ WS2/Mg掺杂ZnO纳米复合材料。 | 罗丹明B (RhB) | 5分钟90% | [98] |
| 2。 | PD-TIO.2光催化剂 | 阿莫西林(AMX) | 5小时内97.5% | [107] |
| 3。 | 六角WS2血小板 | 若丹明B | 98%, 105分钟 | [99] |
| 4. | Ag)+、铁3+和锌2+插层镉(II)金属有机框架 | 2-胆红素(2CP) | 93%在5 h | [104] |
| 5。 | 还原氧化石墨烯和Ag包覆的TiO2 |
双酚A (BPA) |
69.1%在5 h |
[105] |
| 6。 | 石墨烯桥接Ag)3.阿宝4/ AG / BIVO4光催化剂 |
四环素 |
60min中的94.96%删除 |
[106] |
7。 |
磁性生物炭支持的g-C3.N4/ FeVO4 |
甲基帕拉根(MEP)和2-胆丙苯酚(2-CP) |
98.4%的MeP去除和 90.7% 2 cp删除 |
[100] |
8。 |
基于IN的MOF /石墨烯氧化物 |
阿莫西林(AMX) |
AMX去除率93%,TOC去除率80% |
[101] |
9。 |
磁性rgo / zno / znfe2O4复合 |
亚甲蓝(MB) |
98.64%在60分钟 |
[102] |
11. |
菲3.O4纳米粒子和草酸盐复合物 |
苯酚 |
3小时内97.61% |
[103] |
12. |
硫化铜锌锡(CZTS)纳米颗粒 | 亚甲基蓝色(MB)染料 | 45分钟50% | [108] |
13。 |
网状的氧化锌 | 酸性红88染料 | 79%, 180分钟 | [109] |
14。 |
α铁2O3.nanosheets |
双酚S | 91%, 120分钟 | [110] |
15. |
Ag / TiO2光催化剂 |
阿莫西林,2,4-二氯苯酚 |
63.48%的AMX和60.23%的2,4- dcp在5h |
[111] |
使用异质催化剂的芬顿反应
在传统的FENTON工艺中,从处理的水中去除溶解的铁是最大的挑战之一,这是促使使用异质催化剂以及FENTON工艺的挑战之一。该研究已经开始使用支持的铁催化剂来减少污泥地层并增加芬顿反应有效的pH范围。在非均相催化剂中,负载的FENTON工艺反应物分子被吸附在存在于催化剂表面上的活性位点上。在反应发生后,产品被解吸。112使用针铁矿(-FeOOH)、赤铁矿(-Fe)2O3.),菲斯2/ SiO2,ilmenite(Fetio3.)和钛磁铁矿(Fe3.TiO4)作为非均相芬顿催化剂已被许多研究者研究。113 - 116理想的多相催化剂的优点是它能与水分离,并且在pH范围广的条件下起作用。使用Fenton/ Heterogeneous催化剂降解的各种污染物如表5所示。
表5:使用Fenton /异质催化剂降解污染物
Sl。 |
芬顿/异构催化剂 |
污染物 |
去除效率 |
参考。 |
1. |
Photo-Fenton/磁铁矿和EDDS |
双酚A (BPA) |
BPA = 70%在11h |
[117] |
2。 |
生物电fenton /碳毡阴极/掺硼金刚石阳极 |
药物废水 |
COD = 60%, 5-氟尿嘧啶= 88%,咖啡因= 43% |
[118] |
3。 |
FENTON / FES.2/ SiO2 |
Ciproflaxacin. |
环丙沙星= 99% 60 min |
[113] |
4. |
芬顿/铁污泥 |
垃圾填埋场渗滤液 |
生化需氧量7= 99%, cod = 86% |
[119] |
5。 |
照片芬顿 |
城市污水中的微污染物 |
微润肤剂= 40% |
[120] |
6。 |
Fenton用石墨烯改性铁污泥作为催化剂 |
罗丹明B (RhB),酸性红G (ARG),甲硝唑 |
RhB = 99%, ARG = 98.5%,甲硝唑= 91.8% |
[121] |
7。 |
用沸石作为催化剂的芬顿氧化 |
扑热息痛 |
扑热息痛去除=〜99%,TOC去除= 60%5h |
[122] |
其他AOP.
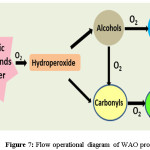
以上讨论的过程是AOPs中最突出的具有实际适用性的过程。除此之外,还有湿空气氧化法(WAO)、超临界湿氧化法(SWOP)和电子束辐射法。在高压和高温环境下,WAO利用分子氧或空气作为氧化剂。这种极端条件会产生自由基来分解废物。123.因此,温度和压力是WAO过程的控制因素。大部分有机酸,不含乙酸和丙酸124.转化为一氧化碳2在高温度。图7描述了湿法氧化的简单功能。
 |
|
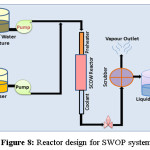
在处理极端反应环境时,需要巨大的运营支出和投资来维持WAO系统。图8说明了WAO系统采用的反应器设计。
 |
|
SWOP采用超临界条件,即在极端的温度和压力条件下,水改变其极性,成为非极性溶剂,与有机部分混溶。在超临界条件下,水可以与氧混合,形成均匀的混合物,是有机物降解的理想介质。当有机化合物和氧在水中溶解在临界点以上时,它们立即在一个单一的均相中进入亲密的分子接触。在足够高的温度下,没有界面输运限制,动力学是快速的,氧化反应迅速进行到完成。这种超临界水氧化(SCOW)也称为水热氧化(HTO)。这一过程使用均匀混合物中的过氧化氢来氧化超过水临界点的有毒废水。如果有机物处于固相,则需要采用多相催化SCOW。它是环境修复中最有效的方法,可完全去除可氧化物质。直到今天,像氨或氰化物这样的无机物也可以转化为一氧化碳2H2O, N2.甲渣由四个步骤组成,从加压试剂,反应,盐分离和减压时。废水和氧化剂混合并在污点反应器中喂食。氧化剂在反应前通常加热,并且该反应条件允许废物和氧化剂之间的放热反应。在氧化反应中获得的热能有助于最佳地使试剂激活至可氧化条件。处理后,由于盐溶解度降低,在反应器内可见盐沉淀。虽然该过程需要高能量,但是可以通过利用这种热流来恢复这种需求,以进行预热或能量产生。在过去几年中,在SCW中深入了解SCW中有机反应的许多作品,在过去几年中已经开发出了对水性质和动力学建模的影响。表6由已纳入污体工厂进行水处理的组织名单。图9显示了水/废水处理的SWOP过程的原理图,而表6列出了包含该组织的组织。
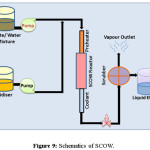 |
|
表6:在水处理方面加入SCOW工厂的一些组织的名单
复合 |
治疗的污水 |
删除效率 |
参考。 |
苏黎世联邦理工学院 (瑞士) |
甲醇 |
TOC REM。99.9% |
[125] |
ITC-CPV Karlsruhe (德国) |
乙醇钠2所以4、造纸厂废水 |
TOC REM。99.9% |
[126] |
桑迪亚的曾经 (美国) |
异丙醇 军用烟和染料配方 |
无Na2SO4沉淀 世界讲述墙 |
[127] |
派恩布拉夫阿森纳 (美国) |
异丙醇 糖和NA2所以4 军事烟雾和染料 配方 |
TOC REM。99.9% |
[128] |
美国海军/陆军杜格威证明 地面设施 (犹他州) |
海军废物(Cl-和Fl-(71小时)化学武器(231小时) |
TOC REM。> 99.9% (蓝草化学武器销毁审判) |
[129] |
CEA(法国) |
甲醇 |
TOC REM。99.9% |
[130] |
结论
该综述明确讨论了广泛用于水管理的各种AOPs的稳健性。它们的处理效率取决于各种工艺参数,这些参数已被清楚地回顾过。然而,由于操作成本高、能耗高、反应物生成少等限制,需要进行工艺强化。强化系统的强度明确了它们在处理各种污染物方面的作用。虽然对水处理的各种AOPs进行了讨论,但多相光催化在实时应用中是最受欢迎的。整体而言,检讨为市民提供了水质和污水处理的可操作性方案。
承认
通讯作者非常感谢科学与工程研究委员会(塞尔维亚),科技部在早期职业研究奖中获得的财政支持,资助代码为ECR/2016/001400。
参考文献
- Akar,S.T.,&Uysal,R.未处理的粘土具有高吸附能力,用于从水溶液中有效去除Ci酸红88:批量和动态流动模式研究。化学工程杂志.2010, 162(2): 591 - 598。
- Biå“,A.K。,&Sobera-MadeJ,S。在废水处理期间去除抗生素物质的晚期氧化过程(UV,UV / H2O2和O3)的比较。臭氧:科学与工程.2012年,34(2):136 - 139。
- 微藻与废水处理。沙特生物科学杂志.2012; 19(3): 257 - 275。
- Tsydenova, O., Batoev, V., & Batoeva, A.太阳能增强高级氧化处理水:同时去除病原体和化学污染物。国际环境研究与公共卫生杂志.2015; 12(8): 9542 - 9561。
- 在鱼类和包括人类在内的其他生物体中,内分泌干扰物(EDCs)、持久性有机污染物(POPs)和其他有机化合物的生物积累和发生。生物积累的新方面和新发展1 - 166)。柏林,海德堡,2000。
- 刘玉华,何小霞,傅玉华,等。羟自由基氧化法降解土霉素的动力学和机理研究。化学工程杂志.2016; 284:1317-1327。
- Ayoub,K.,Van Hullebusch,E。D.,Cassir,M.和Bermond,A。在删除TNT清除的先进氧化过程的应用:审查。危险材料杂志。2010; 178(1):10-28。
- Bebelis, S., Bouzek, K., Cornell, A., Ferreira, M. G. S., Kelsall, G. H., Lapicque, F., & Walsh, F. C.电化学工程发展中的亮点。化学工程研究与设计.2013; 91(10):1998-2020。
- Bethi,B.,Sonawane,S.H.,Bhanvase,B.A。,Gumfekar,S。纳米材料的纳米材料的污水处理氧化方法:综述。化学工程与加工:过程强化.2016; 109:178-189。
- Fernándezâ€Castro, P., Vallejo, M., San Román, M., & Ortiz, I.高级氧化过程的基本原理。活性氧测定方法的作用与评述。化学技术与生物技术学报.2015, 90(5): 796 - 820。
- 用臭氧处理饮用水。环境科学与技术.1987; 21(3): 224 - 230。
- 釉,W.H.,康,J.W.,&Chapin,D.H。水处理过程的化学涉及臭氧,过氧化氢和紫外线辐射。1987年。
- 陈志强,陈志强,陈志强,等。高阶氧化过程中声光催化的研究进展[j]。超声波Sonochemisty.2009; 16(5): 583 - 589。
- Chowdhury,P.和Viraraghavan,T.氯化有机化合物,酚类化合物和有机染料的多人化学降解 - 综述。全环境科学.2009; 407:2474-2492。
- Sathishkumar,P.,Mangalaraja,R. V.,&Anandan,S.近期经说Sonochemical和合并的儿童氧化过程改进的审查 - 一种销毁环境污染物的强大工具。可再生和可持续能源评论.2016; 55:426 - 454。
- 陈志强,陈志强,陈志强,等。一种制备纳米悬浮体的新技术。超声波Sonochemisty.2007; 14:519 - 530。
- Doosti,M. R.,Kargar,R.,&Sayadi,M. H.使用超声援助的水处理:审查。国际生态学与环境科学院的诉讼程序.2012; 2(2): 96 - 110。
- 超声波和生物催化剂的结合:从水溶液中去除2-氯酚。超声波Sonochemisty.2006; 13:37-41。
- 陈志强,陈志强。超声波技术在水处理中的应用。伊朗公共卫生杂志.38(2): 17。
- Tuziuti, K. Yasui, Y. Iida, H. tada, S. Koda,超声波.2009; 42(1-9),(2004)597-601。
- 声解光催化降解偶氮染料的协同效应。物理化学.2002; 4(24), 6123 - 6128。
- 脉炎,C.D.,Lesko,T.,Colussi,A.J.,Hoffmann,M.R.,在臭氧存在下含水生物氧态的Sonamytic分解。J. Phy。化学。Ag)ydF4y2Ba2010; 114:4968E4980。
- 王,X.,王,J.,Guo,P.,Guo,W.和Wang。C.,通过使用旋转喷射诱导的空化与H 2 O 2结合水溶液中罗丹明B的降解。危险材料杂志.2009; 169:486 - 491。
- 丁志刚,王志刚,王志刚,等。声解法与臭氧解法协同氧化偶氮苯和甲基橙的研究。J. Phy。化学。Ag)ydF4y2Ba.2000; 104:8930e8935。
- 引用本文:王文辉,康建伟,张志强,等。臭氧、过氧化氢和紫外线辐射对水处理过程的影响。1987年。
- 饮用水的臭氧化:第一部分氧化动力学和产物形成。水研处.2003; 37(7):1443-1467。
- Konsowa,A。H.在批量泡泡柱反应器中臭氧化含有直接染料的废水的脱色。海水淡化.2003; 158(1):233-240。
- Hoigné,J.含臭氧水化学和污染物的转化,臭氧化和先进的氧化过程。在饮用水的质量和治疗中II:83-141。Springer Berlin Heidelberg。1998年。
- Borowska Bourgin, M, E,海尔宾,J。,Hollender J。,凯撒,H . P。Kienle, C,和冯·Gunten美国运营和水质的影响参数对常规臭氧化和先进的氧化过程O 3 / H 2 O 2:动力学的微量污染物减排、转换产品和溴酸盐形成地表水。水的研究.2017; 122:234-245。
- GOTTSchalk,C.,Libra,J.A.和Saupe,A.臭氧化水和废水:了解臭氧及其应用的实用指南。约翰瓦里和儿子。2009年。
- 在饮用水处理中使用臭氧和相关的氧化过程。水科学进展,32(11):3208-3222。(1998)
- Badia-Fabregat,M.,Oller,I.和Malato,S。概述试验规模治疗和医院流出物的新型和创新技术。(2017)。
- 在有机溶质作为自由基链反应的促进剂和抑制剂存在的情况下,臭氧在水中的分解。环境科学与技术,19(12):1206-1213。(1985)
- 王志强,王志强,王志强,等。水溶液中臭氧与e-aq、2- (1-)(O2-)和质子反应的速率常数和产物。物理化学学报,26(11):1409 - 1409。(1983)
- Stetller,R.,Courbat,R.,Von Gunten,U.,Kaiser,H.P.P.,Walther,J.L.,Gaille,P.和Revelly,P.利用DE L'Ozone Pour Le Traitements Des Eaux Poteles en Suisse。GWA,78(11):876-890。(1998)
- 化学资料的相关分析。施普林格。(1988)
- 水化学,第三。John Wiley and Sons,纽约。(1996)
- 蓝藻毒素:饮用水处理过程中的清除和人类风险评估。环境卫生展望,108(增刊1),113。Hoigné, J.,和Bader, H.(1983)。臭氧在水中与有机和无机化合物反应的速率常数- ii:分解有机化合物。水资源研究,17(2):185-194。(2000)
- Haag,W. R.和YaO,C.D。羟基自由基与几种饮用水污染物反应的速率常数。环境科学与技术,26(5):1005-1013。(1992)
- 3 .陈志强,陈志强,陈志强,等。臭氧与乙烯及其甲基和氯取代衍生物在水溶液中的反应。环境科学与技术,32(8):1112-1119。(1998)
- Muñoz,F.和von Sonntag,C.臭氧与叔胺的反应,包括络合剂亚硝基酰基乙酸(NTA)和水溶液中的乙二胺四乙酸(EDTA)。化学学会,Perkin交易2,(10):2029-2033。(2000)
- 陈志强,陈志强,陈志强,等。臭氧氧化和高级氧化过程中药物的氧化。环境科学与技术,37(5):1016-1024。(2003)
- Pryor,W. A.,Giamalva,D. H.和Church,D. F. F. ozonation的动力学。2.水中氨基酸和模型化合物和非极性溶剂率的比较。美国化学学会,106(23):7094-7100。(1984)
- Muñoz,F.,Mvula,E.,Braslavsky,S.和von Sonntag,C.在水溶液中的臭氧反应中的单态二恶英形成。化学学会,Perkin交易2,(7):1109-1116。(2001)
- Rennecker,J.L,Mariñas,B.,欧文斯,J.H,J.H和Rice,E. W. W.用臭氧灭活的Cryptosporidium parvum卵囊的灭活。水研究,33(11):2481-2488。(1999)
- Reunggoat,J.,Escher,B. I.,Macova,M.和Keller,J.污水处理厂的生物滤膜植物流出物:有效去除药物和个人护理产品和减少毒性。水研究,45(9):2751-2762。(2011)
- 高级氧化工艺(AOP)用于水的净化和回收。催化今天,53(1):51-59。(1999)
- Duguet, j.p, Brodard, E., Dussert, B., and Mallevialle, J.,通过过氧化氢的使用改善饮用水臭氧化效果。(1985)
- Pinkernell,U.和Von Gunten,U.在臭氧层化期间最小化溴化物最小化:机械考虑。环境科学和技术,35(12):2525-2531。(2001)
- 引用本文:王文辉,康建伟,张志强,等。臭氧、过氧化氢和紫外线辐射对水处理过程的影响。(1987)
- 李志强,李志强,李志强,等。集成电路生产中废水处理技术的研究进展。引用本文:王志强,王志强,王志强。(1981)
- Bollyky,L. J.试点植物研究使用臭氧和臭氧 - 过氧化氢的THM,味道和气味控制。臭氧在水和废水处理中的作用。第二届国际会议的诉讼程序。DW Smith和GR Finch,EDS。((1987年):(1987年)
- 臭氧-过氧化氢结合对有机物的氧化作用。(1984)
- Duguet, j.p, Brodard, E., Dussert, B., and Mallevialle, J.,通过过氧化氢的使用改善饮用水臭氧化效果。(1985)
- 高级氧化工艺的现状与展望。爱沙尼亚学会科学。化学、50(2):59 - 80。(2001)
- Cortes,S.,Sarasa,J.,Ormad,P.,Gracia,R.和Ovelleiro,J.L。系统O3 /高pH和O 3 /催化剂的氯苯氧化在水中的比较效率。臭氧:科学与工程,22(4):415-426。(2000)
- 丁酸催化臭氧化反应的动力学研究。Int。Reg。臭氧化和AOPs在水处理中的应用。即将于9月23日至25日。(1998)
- 刘志强,刘志强,刘志强,等。臭氧化对GAC性能的影响。在汽车牌照。臭氧,紫外线,AOPs水处理。,年代eptember 24–26, 1996, Amsterdam, Netherlands: 307-318. (1996)
- 水中药物的氧化处理。水科学进展,34(6):1881-1885。(2000)
- Valdés, H., Schrickel, K., Bormann, H., and Sievers, M. Ozonation of pentylacetate pollution water from textile care industry。(13)。(2013)
- Legrini,O.,Oliveros,E.和Braun,A.M.水处理的光化学方法。化学评论,93(2):671-698。(1993)。
- 马塔西,R., Weston, R., Lau, P., Cruver, J., Marek, S., & Tomowich, D.(1999)。废水技术概况:紫外线消毒,美国环境保护署,水办公室,华盛顿特区。环保局832 - f - 99 - 064。
- Giller,H.F.J.I,综述灯具类型,诉讼消毒2000.水环境联合会,(2000)。
- 废水紫外线消毒。从iwa-network.org检索。
- 李春华,崔文英,金玉刚,尹建军,二亚硝基二甲胺在水中的紫外光解机理:甲胺和二甲胺的双途径合成。环绕。科学。抛光工艺。39岁,2101 - 2106。(2005)
- 李志强,李志强,李志强,等。n -亚硝基二甲胺在水中的UV光解机理研究进展。科学。抛光工艺。39岁,9702 - 9709。(2005)
- 中压和低压汞灯的实验和模型比较2O2模拟饮用水中n -亚硝基二甲胺的紫外光降解。环绕。科学。抛光工艺。37:1933 - 1940。(2003)。
- Sakai,H.,Takamatsu,T.,Kosaka,K.,Kamiko,N和Takizawa,S.波长和水质对N-硝基甲酰基甲胺(NDMA)的光降解的影响。ChemoSphere,89(6):702-707。(2012)。
- Sanches,S.,Crespo,M.T. B.,&Pereira,V. J.使用低压UV光解和晚期氧化过程的优先杀虫剂的饮用水处理。水研究,44(6),1809-1818。(2010)
- Kim,I.,Yamashita,N.和Tanaka,H.紫外线和紫外线/ h的性能2O2日本某污水处理厂二级出水中检测到的药品的去除工艺。中国环境科学,2019,30(2):427 - 434。(2009)。
- Avisar,D.,Lester,Y.和Mamane,H.PH诱导的多色UV处理,用于去除SMX,OTC和CIP的混合物。危险材料杂志,175(1):1068-1074。(2010)。
- Real, F. J., Benitez, F. J., Acero, J. L., Sagasti, J. J., and Casas, F.在超纯和自然水体中化学氧化药物primidone,酮洛芬和泛atrizoate的动力学。工业与工程化学,48(7):3380-3388。(2009)。
- BÅ, Ä™dzka, D., Gmurek, M., Gryglik, M., Olak, M., Miller, J. S.和Ledakowicz, S.水溶液中内分泌干扰物的光降解和高级氧化。催化学报,31(1):125-130。(2010)。
- BÅ, Ä™dzka, D., Gmurek, M., Olak-Kucharczyk, M., Miller, J. S., and Ledakowicz, S. Sulejow水库天然水中对尼苯金正丁酯的光降解。化学。Eng。s2012a, 19: 517-25。(2011)。
- Hassaan,M. A.和EL NEMR,A.纺织废水处理的先进氧化方法。国际光化学和光学生物学杂志,2(3):85-93。(2017)。
- Rao,Y. F.和Chu,W。用UV,Ozonation和UV / O量化Linuron降解动力学的新方法3.光化层,74(11):1444 - 1449。(2009)。
- 高级氧化工艺的现状与展望。爱沙尼亚学会科学。化学、50(2):59 - 80。(2001)。
- Tehrani-Bagha,A. R.和Amini,F. L.通过UV增强的臭氧化反应性染料的脱色。颜色,着色剂和涂层的进展,3:1-8。(2010)。
- Hassaan,M. A.,El Nemr,A.和Madkour,F. F. F. F. F.测试了对废水中直接蓝86染料的降解的先进氧化过程。埃及水产研究杂志,43(1):11-19。(2017)。
- Hassaan,M. A.,El Nemr,A.,And Madkour,F. F. F.淡水和海水中摩尔紫罗兰40染料的先进氧化过程。埃及水生研究杂志,43(1):1-9。(2017)。
- 臭氧和紫外线辅助臭氧在海水中对直接黄50脱色中的应用。药物化学,ISSN: 2349-7092, 3(3):131-138。(2016)。
- 龚军,刘艳,孙旭东3.和紫外/ O3.城市污水生物处理后有机成分的氧化。水科学进展,42(4):1238-1244。(2008)。
- 卢卡斯,M. S.,佩雷斯,J.A。和Puma,G.L。基于臭氧的先进氧化过程处理酿酒厂废水(O.3.阿,3./紫外线和O3./ UV /小时2O2)在试验型泡泡柱反应器和过程经济学中。分离和纯化技术,72(3):235-241。(2010)。
- Souza,F. S.和Féris,L. A。通过先进的氧化过程降解咖啡因:O.3.和O3./紫外线。臭氧:科学与工程,37(4):379-384。(2015)。
- Rao,Y. F.和Chu,W。用UV,Ozonation和UV / O量化Linuron降解动力学的新方法3.光化层,74(11):1444 - 1449。(2009)。
- Chen,Z.,Fang,J。,风扇,C.和Shang,C.通过臭氧/紫外线方法进行N-亚硝基吡咯烷的氧化降解:动力学和途径。化学影像层,150:731-739。(2016)。
- 模拟和真实城市废水中双酚A的UV氧化,O3.和紫外/ O3..海水淡化与水处理,57(3):1075-1083。(2016)。
- Barik,A. J.和Gogate,P. R.使用基于超声,光解和臭氧的组合策略降解4-氯-2-氨基酚。超声波Sonochemistry,28:90-99。(2016)。
- Fenton,H.J.H.在铁的存在下在铁酸的氧化。化学学会,交易,65:899-910(1894年)
- 王志强,王志强,王志强,等。铁盐催化过氧化氢分解的研究进展。伦敦皇家学会学报A辑:数学、物理与工程科学,147(861):332-351 (1934)
- 高级氧化工艺的现状与展望。爱沙尼亚学会科学。Chem,50(2):59-80(2001)
- 王志强,王志强,王志强,等。双氧水与亚铁和铁离子的化学反应。大自然,163(4148):692-694(1949)
- 王志强,王志强,王志强,等。双氧水与亚铁和铁离子的化学反应。第一部分:亚铁离子反应。法拉第学会学报,47:462-500 (1951a)
- 王志强,王志强,王志强,等。双氧水与亚铁和铁离子的化学反应。第二部分。- 铁离子反应。法拉第协会的交易,47:591-616(1951B)
- 围墙,C. Fenton的试剂重新审视。化学研究的叙述,8(4):125-131(1975)
- 王志强,王志强,王志强,等。Fenton试剂氧化乙醇的研究进展。铜离子的影响。美国化学学会学报,93(17):4275-4281 (1971)
- Pignatello,J.J.,Oliveros,E.,&Mackay,A.基于Fenton反应和相关化学的有机污染物破坏的先进氧化过程。环境科学与技术的关键评论,36(1):1-84(2006)
- 陈志强,陈志强,陈志强,等。Fenton法和光Fenton法降解苯酚的研究进展。地球化学,55(9):1235-1243 (2004)
- 利用纳米级零价铁对难降解工业废水进行芬顿氧化研究。acta photonica sinica, 2012, 40(4): 457 - 462。(2012)。
- 陈永强,王安生,张永强,王安生,田晓丽,李建军。电fenton法降解抗生素环丙沙星(CIP)的研究进展:Fe3+-CIP螯合物的形成及其对Fe2+/Fe3+催化行为和CIP矿化的影响。电化学学报,32(6):851 - 856。(2017)。
- 王,N.,Jia,D.,Jin,Y.,Sun,S.P.,&Ke,Q.通过NTA / EDTA在循环pH下通过NTA / EDTA增强了FENTON样的TCE中的TCE。环境科学与污染研究,24(21):17598-17605。(2017)。
- Bertrand,R. L.铁积累,谷胱甘肽耗尽和脂质过氧化必须在冻死期间同时发生,并且是相互放大的事件。医学假设,101:69-74。(2017)。
- Gogoi,A.,Navgire,M.,Sarma,K.C.,&Gogoi,P.新型高度稳定的β-环糊精富勒烯混合价Fe-Metal框架,用于快速芬芳的茜素降解。RSC推进,7(64):40371-40382。(2017)。
- 陈志强,陈志强,陈志强,等。水溶性聚合物的光- fenton去除技术研究进展。化学工程与加工:过程强化,47(12):2361-2369。(2008)。
- Khataee, Salahpour, F。,Fathinia, M, Seyyedi, B。,B &瓦希德。铁丰富的红土土壤与介孔结构异构Fenton-like降解偶氮染料的可见光。工业化学学报,26:129-135。(2015)。
- 陈志强,陈志强,陈志强,等。UV和中性光fenton对活性污泥处理生活污水中32种污染物的降解作用。水科学进展,46(6):1947-1957。(2012)。
- 王志强,王志强,王志强,等。Fenton试剂降解甲基叔丁基醚的研究进展。环境科学与技术,2003,23(4):427 - 434。水科学进展,39(1):107-118。(2005)。
- KoäAnová,V.,&Dušek,L.钢的电化学溶解作为电芬氧化的典型催化剂。MonatshefteFürchemie-化学月,147(5),935-941。(2016)。
- Abdelaziz, a.a., Nosier, s.a., & Hussien, M.使用electroâ€Fenton技术处理含酚工业废水。环境工程学报,2(5):47-59。(2015)。
- Beqqal,N.,Yahya,M.S.,Karbane,M.E.E.E.E.E.L.,宫,A.,&El Kacemi,K。通过电芬顿葡萄糖素药物污染的水溶液降解/矿化的动力学研究:实验参数的影响。材料与环境科学,8(12):4399-4407。(2017)。
- Asghar,A.,Salihoudin,A.,Aziz Abdul Raman,A.,&Mohd Ashri Wan Daud,W.阴极改性,提高了Microbial燃料电池中的芬顿氧化的性能。环境进步与可持续能源,36(2):382-393。(2017)。
- 陈志强,王志强,陈志强,等。Fenton法光辅助Fenton法处理印染废水的研究进展。海水淡化,269(1):1 - 16。(2011)。
- 赵志华,徐晓蓉,李国栋,刘建军,孔丽娟,左丽珍。FeS2/SiO2微球催化降解环丙沙星的动力学、反应途径和机理。材料科学与工程学报,31(6):457 - 461。(2017)。
- 林志荣,赵磊,董永华。低分子量有机酸和黄腐酸对fenton - fenton催化降解三氯二苯并生成羟基的影响。化学工程学报。(2017)。
- 黄晓东,侯旭东,贾凡,宋凡,赵军,&张磊。抗坏血酸促进的表面铁循环对非均相Fenton甲草胺的高效降解。材料科学与工程,2019,47(5):531 - 534。(2017)。
- 陈志强,陈志强,陈志强,等。钛铁矿催化Fenton反应降解II型橙的研究。环境科学与技术,24(7):6187-6194。(2017)。
- 黄,W.,Luo,M.,Wei,C.,Wang,Y.,Hanna,K。和Mailhot,G.通过磁铁矿和EDDS改性的增强的异构照片 - Fenton方法:BPA降解。环境科学与污染研究,24(11):10421-10429。(2017)。
- 生物电fenton:生物-高级氧化联合处理制药废水的评价。环境科学与污染研究:1-10(2017)。
- 基于Fenton-like工艺的垃圾渗滤液生物-化学处理研究。环境科学学报,19(2):541-551。(2017)。
- Villegas-Guzman, P., Giannakis, S., Rtimi, S., Grandjean, D., Bensimon, M., De Alencastro, L. F., Torres-Palma, R., & Pulgarin, C. A green solar photo-Fenton process for the elimination of bacteria and micropollutants in municipal wastewater treatment using mineral iron and natural organic acids. Applied Catalysis B: Environmental, 219: 538-549. (2017).
- 郭,科,元,N.,张,G.,&Jimmy,C. Y. Y.石墨烯改性铁污泥衍生自均匀Fenton工艺作为有效的有机污染物降解的有效的异构Fenton催化剂。微孔和中孔材料,238:62-68。(2017)。
- Velichkova,F.,Delmas,H.,Julcour,C.,&koumanova,B.异构Fenton和Fenton氧化用于使用含有Zsm的铁除去催化剂的铁淀粉酰胺去除。Aiche Journal,63(2):669-679。(2017)。
- Mishra,V.S.,Mahajani,V.V.V.,Joshi,J.B。湿空气氧化。工业与工程化学研究,34(1),2-48。(1995)。
- Debellefontaine,H.,Chakchouk,M.,Foussard,J.N.,Tissot,D.和Striolo,P.治疗有机含水废物:湿式空气氧化和湿过氧化物氧化氧化。环境污染,92(2),155-164。(1996)。
- Wellig,B。,Lieball,K。,&von Rohr,P. R.与内部热源具有水热火焰的转子壁Scwo反应器的操作特性。超临界流体杂志,34(1),35-50。(2005)。
- 张凡,马建军,马建军。壁式SCWO反应器的CFD模拟:水膜的形成与优化。农业科学学报,62(1),195-206。(2016)。
- 大米,吴,吴,B.C.,Winters,W.S.,&Robinson,C。D.松木诈鲁武器超临界水氧化反应器的工程建模(No. Sand2000-8656C)。桑迪亚国家实验室。,阿尔伯克基,纳米和利弗雷,加利福尼亚州(美国)。(2000)。
- Ahluwalia KS, Crooker P, Meagher GM. Blue Grass化学武器销毁的蒸腾壁SCWO技术演示。超临界水氧化技术在商业应用中的成就和挑战研讨会论文集,弗吉尼亚州阿灵顿,8月15日;(2001)。
- FAUVEL,E.,Joussot-Dubien,C.,Guichardon,P.,Charbist,G.,Charbit,F.,&Sarrade,S。一种用于水热氧化的双壁反应器,具有穿过内部多孔管的超临界水流。超临界流体杂志,28(1),47-56。(2004)。
- Bermejo,M. D.,Fdez-Polanco,F.,Cocero,M. J. J. Transpiring Wall对超临界水氧化反应器的行为的影响:建模和实验结果。工业与工程化学研究,45(10),3438-3446。(2006)。

这个作品是根据知识共享署名4.0国际许可.








